本文
新型コロナウイルス感染症における抗ウイルス薬等の医療機関での取り扱いについて
| ゾコーバの一般流通が開始されましたので、令和5年3月31日以降、通常の医薬品と同様の取り扱いとなります。 |
|---|
| コロナの院内感染が発生した場合には、当該病院自身が、自院入院中の陽性患者に、抗ウイルス薬を投与する必要性が生じます。 早期の投与ができるよう、未発生のうちに、抗ウイルス薬の配分を受ける医療機関としての「センター登録」と、薬の確保をご検討ください。 |
新型コロナウイルス感染症の治療薬として承認されている抗ウイルス薬等の取り扱いに関する医療機関様向けページになります。
なお、抗ウイルス薬については、PCR検査を実施せずに、抗原定量検査や抗原定性検査でSARS-CoV-2感染が確認された場合は、当該検査結果の有効性などを踏まえて、検査結果に基づき医師による確定診断が行われれば、処方することが可能です。
【次の医薬品に関する取り扱い等を記載】
「モルヌピラビル」(販売名:ラゲブリオ):令和3年12月24日に特例承認されました。
「ニルマトレルビル・リトナビル」(販売名:パキロビッド):令和4年2月10日に特例承認されました。
「レムデシビル」(販売名:ベクルリー): 令和2年5月7日に特例承認されました。
「チキサゲビマブ及びシルガビマブ」(販売名:エバシェルド):令和4年8月30日に特例承認されました。
「エンシトレルビルフマル酸」(販売名:ゾコーバ):令和4年11月22日に緊急承認されました。
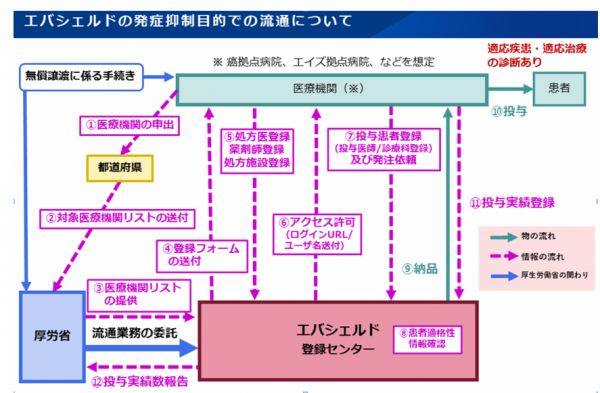
現状、中和抗体薬のエバシェルドについては、安定的な供給が難しいことから、一般流通は行わず、当面の間、国が所有した上で、発症抑制目的での投与についてのみ、製薬会社が設置する「登録センター」に登録した医療機関に無償で提供されます。
なお、ベクルリーは、令和3年10月18日から、ラゲブリオは、令和4年9月16日から、パキロビットは、令和5年3月22日から、ゾコーバは、令和5年3月31日から、一般流通が開始され、登録等の手続きは不要のため、直接、医薬品卸売販売業者にお尋ねください。
1 モルヌピラビル(販売名:ラゲブリオ®カプセル200mg)
(1)投与対象となる方
現在承認されている経口治療薬の投与の対象となるのは、次の条件を満たす場合で、医師が必要と判断した方です。患者の方すべてに投与できるわけではありません。
- 本剤の成分に対し過敏症の既往歴がないこと。
- 18歳以上であること。
- 妊婦でない又は妊娠している可能性がないこと。
- 次の重症化リスク因子を少なくとも一つ有していること。
重症化リスク因子について、詳しくは、令和3年12月24日(令和4年8月15日最終改正)新型コロナウイルス感染症対策推進本部及び医薬・生活衛生局総務課事務連絡「新型コロナウイルス感染症における経口治療薬(ラゲブリオ®カプセル)の医療機関及び薬局への配分について」の別紙1の2の〇1〇2に記載の重症化リスク因子をご確認ください。
〇上記通知の別紙1の2の〇1〇2で挙げられている重症化リスク因子(抜粋)
(ア)日本感染症学会の「COVID 19 に対する薬物治療の考え方 第15報」(2022年11月22日)の記載に基づく情報
(イ)承認審査における評価資料となった国際共同第2/3相試験(MOVeOUT(002)試験)の組み入れ基準、新型コロナウイルス感染症に係る国内の主要な診療ガイドラインである「新型コロナウイルス感染症(COVID19)診療の手引き 第8.1版」(令和4年10月5日)以下、「診療の手引き 第8.1版」)、既に承認を受けている英国で、臨床試験(PANORAMIC試験)の組み入れ基準において例示されている重症化リスク因子として想定
(いずれも処方にあたっては最新の情報をご確認ください。)
- 61歳以上
- 活動性の癌(免疫抑制又は高い死亡率を伴わない癌は除く)
- 慢性腎臓病
- 慢性閉塞性肺疾患
- 肥満(BMI30kg/m2以上)
- 重篤な心疾患(心不全、冠動脈疾患又は心筋症)
- 糖尿病
- ダウン症
- 脳神経疾患(多発性硬化症、ハンチントン病、重症筋無力症等)
- コントロール不良のHIV感染症およびAIDS
- 肝硬変等の重度の肝臓疾患
- 臓器移植後、骨髄移植、幹細胞移植後
- 高血圧
- 脂質異常症
- 喫煙
- 固形臓器移植後の免疫不全
- 慢性的な心臓または血管の病気
- 慢性的な肝疾患
- 慢性神経疾患(認知症、脳卒中、てんかんを含む)
- 重度の学習障害
- 重度の精神疾患
- 臨床医又は看護師が臨床的に脆弱と判断した場合 など
〇「診療の手引き 第8.1版」において、臨床試験における主な投与知見が示されており、意義が大きいと考えられている重症化リスク因子
下表を参照してください
(2)その他
- 9月16日以降の院内又は薬局内在庫として保有する国購入品の取り扱いについて
令和3年12月24日(令和4年8月15日最終改正)厚生労働省新型コロナウイルス感染症対策推進本部及び医薬・生活衛生局総務課事務連絡「新型コロナウイルス感染症における経口治療薬(ラゲブリオ®カプセル)の医療機関及び薬局への配分について」に基づき患者に投与が可能です。
チェックリスト等取り扱いが変更している点もありますので、令和4年9月15日付厚生労働省新型コロナウイルス感染症対策推進本部、医薬・生活衛生局総務課及び同局医薬品審査管理の事務連絡「新型コロナウイルス感染症における経口治療薬(ラゲブリオ®カプセル)の薬価収載に伴う医療機関及び薬局への配分について(その3)」も確認してください。
医務保険課HP(https://www.pref.yamaguchi.lg.jp/soshiki/46/18932.html)
- 同意書ひな型について
ラゲブリオ®TOP - MSD Connect(https://www.msdconnect.jp/products/lagevrio/<外部リンク>)ホームページ内下段の「医療関係者サポート」に掲載されています。
- 高齢者施設における対応について
高齢者施設においては、通常の医薬品と同様医療機関の往診等や卸売販売業者を通じて購入していだけます。
2 「ニルマトレルビル・リトナビル」(販売名:パキロビッド®パック)
(1)投与対象となる方
現在承認されている経口治療薬の投与の対象となるのは、次の条件を満たす場合で、医師が必要と判断した方です。患者の方すべてに投与できるわけではありません。
- 本剤の成分に対し、重篤な過敏症の既往歴がないこと。
- 成人または12歳以上かつ体重40kg以上の小児であること。
- 併用禁忌の薬剤を投与していないこと。
- 腎機能または肝機能障害のある患者については、コルヒチンを投与していないこと。
- 次の重症化リスク因子を少なくとも一つ有していること。
重症化リスク因子については、令和4年2月10日(令和4年9月27日最終改正)新型コロナウイルス感染症対策推進本部及び医薬・生活衛生局総務課事務連絡「新型コロナウイルス感染症における経口治療薬(パキロビッド®パック)の医療機関及び薬局への配分について」の別紙1の2の〇1〇2をご確認ください。
〇上記通知の別紙1の2の〇1〇2で挙げられている重症化リスク因子(抜粋)
(ア)日本感染症学会の「COVID 19 に対する薬物治療の考え方 第15報」(2022年11月22日)の記載に基づく情報
(イ)承認審査における評価資料となった国際共同第2/3相試験(C4671005(EPIC-HR)試験)の組み入れ基準、新型コロナウイルス感染症に係る国内の主要な診療ガイドラインである「診療の手引き 第8.1版」で想定
(いずれも処方にあたっては最新情報をご確認ください。)
- 60 歳以上
- BMI 25kg/m2超
- 喫煙者(過去 30 日以内の喫煙があり、かつ生涯に 100 本以上の喫煙がある)
- 免疫抑制疾患又は免疫抑制剤の継続投与
- 慢性肺疾患(喘息は、処方薬の連日投与を要する場合のみ)
- 高血圧の診断を受けている
- 心血管疾患(心筋梗塞、脳卒中、一過性脳虚血発作、心不全、ニトログリセリンが処方された狭心症、冠動脈バイパス術、経皮的冠動脈形成術、頚動脈内膜剥離術又は大動脈バイパス術の既往を有する)
- 1型又は 2型糖尿病
- 慢性腎臓病
- 神経発達障害(脳性麻痺、ダウン症候群等)又は医学的複雑性を付与するその他の疾患(遺伝性疾患、メタボリックシンドローム、重度の先天異常等)
- 限局性皮膚がんを除く活動性の癌
- 医療技術への依存( SARS -CoV -2による感染症と無関係な持続陽圧呼吸療法 等)
- 鎌状赤血球症
- 悪性腫瘍
- 慢性呼吸器疾患(COPDなど)
- 糖尿病
- 脂質異常症
- 脳血管疾患
- 喫煙
- 固形臓器移植後の免疫不全
- 妊娠後半期
- 免疫抑制・調整薬の使用
- HIV感染症(特にCD4<200/μL) など
〇「診療の手引き 第8.1版」で臨床試験における主な投与知見が示されている重症化リスク因子
下表を参照してください。
(2)その他
- 3月22日以降の院内又は薬局内在庫として保有する国購入品の取り扱いについて
令和4年2月10日(令和5年3月3日最終改正)付け厚生労働省新型コロナウイルス感染症対策推進本部及び医薬・生活衛生局総務課事務連絡「新型コロナウイルス感染症における経口治療薬(パキロビッド®パック)の医療機関及び薬局への配分について」に基づき患者に投与可能です。
チェックリスト等取り扱いが変更している点もありますので、令和5年5月22日付け厚生労働省新型コロナウイルス感染症対策本部、医薬・生活衛生局総務課の事務連絡「新型コロナウイルス感染症における経口抗ウイルス薬(パキロビッドRパック)の取扱いについて(所有権の移転および再譲渡)」も確認してください。
薬務課HP(https://www.pref.yamaguchi.lg.jp/soshiki/48/20482.html)
- 同意書ひな型について
ファイザー新型コロナウイルス『治療薬』医療従事者専用サイト(https://www.covid19oralrx-hcp.jp/<外部リンク>)内中段<医療関係者サポート>の「パキロビッドによる治療に係る同意書説明文書」をご覧ください。
- 高齢者施設における対応について
高齢者施設においては、通常の医薬品と同様医療機関の往診等や卸売販売業者を通じて購入していただけます。
3 レムデシビル(販売名:ベクルリー点滴静注用100mg)
(1)投与対象となる方
投与の対象となるのは、次の条件を満たす場合で、医師が必要と判断した方です。患者の方すべてに投与できるわけではありません。
- 軽症でも重症化リスク因子(※)を有する方
- 肺炎を発症している方
※重症化リスク因子
- 60歳以上
- BMI30kg/m2以上
- 慢性腎臓病
- 糖尿病
- 免疫抑制
- 心血管疾患、高血圧、脳血管疾患
- 慢性肺疾患
- 慢性肝疾患
- 活動性の癌、鎌状赤血球症 など
(厚生労働省の「診療の手引き・第8.1 版」の記載に基づく情報です。処方にあたっては最新情報をご確認ください。)
4 チキサゲビマブ及びシルガビマブ(販売名:エバシェルド筋注セット)
(1)エバシェルド登録センターへの登録について
- 本剤の処方等を行う医療機関は、本剤を扱う前に、県に申し出てください。
- 申し出後、県及び国を経由し、製造販売業者から登録フォームが送付されますので、医療機関は、「エバシェルド登録センター」に登録してください。
具体的な登録方法・依頼方法については、下記の製品サイト又は製造販売業者が開設するWebサイト「エバシェルド登録センター」(電話番号:0120-162-283)まで、お電話ください。
エバシェルド製品サイト(https://med.astrazeneca.co.jp/evu.html<外部リンク>)
(2)本剤の発注等について
- 投与対象患者への投与予定が決まったら、エバシェルド登録センターから、投与患者情報を登録及び発注をかけてください。
- 現時点、発症抑制目的に限って配分をするものであり、計画的な投与が可能であることから、在庫配置は認められていません。対象者への投与分は都度発注となります。
※営業日の15時までに発注した場合、土日祝日を除き原則翌日までに配送されます。
発注手続き、配送等のお問い合わせ先
エバシェルド登録センター
受付時間:9時から17時30分(土日祝日及び製造販売業者休日を除く)
電話番号:0120-162-283
(3)投与対象となる方
投与対象となる方は、以下のA~Cをすべて満たし、医師が必要と判断した方です。
- 成人又は12歳以上かつ体重40kg以上の小児
- SARS-CoV-2による感染症に対するワクチン接種が推奨されない者又は免疫機能低下等によりSARS-CoV-2による感染症に対するワクチン接種で十分な免疫応答が得られない可能性がある者
- 抗体産生不全あるいは複合免疫不全を呈する原発性免疫不全症の患者
- B細胞枯渇療法(リツキシマブ等)を受けてから1年以内の患者
- ブルトン型チロシキンナーゼ阻害薬を投与されている患者
- キメラ抗原受容体T細胞レシピエント
- 慢性移植片対宿主病を患っている、又は別の適応症のために免疫抑制薬を服用している造血細胞移植後のレシピエント
- 積極的な治療を受けている血液悪性腫瘍の患者
- 肺移植レシピエント
- 固形臓器移植(肺移植以外)を受けてから1年以内の患者
- T細胞又はB細胞枯渇剤による急性拒絶反応で最近治療を受けた固形臓器移植レシピエント
- CD4Tリンパ球細胞数が50cells/μL未満の未治療のHIV患者
(日本感染症学会の「COVID 19に対する薬物治療の考え方 第15版」(2022年11月22日)の記載に基づく情報です。処方にあたっては最新情報をご確認ください。)
- SARS-CoV-2による感染症患者の同居家族又は共同生活者等の濃厚接触者でない者
※SARS-CoV-2による感染症患者の同居家族又は共同生活者等の濃厚接触者における有効性は示されていません。
(4)その他
質疑応答等については、令和4年9月7日(令和4年11月22日最終改正)厚生労働省新型コロナウイルス感染症対策推進本部事務連絡「新型コロナウイルス感染症における中和抗体薬「チキサゲビマブ及びシルガビマブ」の医療機関への配分について」の最新通知をご参照ください。
医務保険課HP(https://www.pref.yamaguchi.lg.jp/soshiki/46/18932.html)
※山口県内のエバシェルド登録済医療機関一覧は以下のPDFファイルをご覧ください
【Evusheld】登録済医療機関一覧 (PDF:145KB)
5 「エンシトレルビルフマル酸」(販売名:ゾコーバ錠125mg。以下「ゾコーバ」)
(1)投与対象となる方
現在承認されている経口治療薬の投与の対象となるのは、次の条件を満たす場合で、医師が必要と判断した方です。患者の方すべてに投与できるわけではありません。
なお、日本感染症学会「COVID-19に対する薬物治療の考え方 第15版」によると、一般に、重症化リスク因子のない軽症例の多くは自然に改善することを念頭に、対症療法で経過を見ることができることから、症状を考慮した上で投与を判断するべきであるとされています。その上で、ゾコーバを投与する場合、臨床試験における成績等を踏まえ、高熱・強い咳症状・強い咽頭痛などの臨床症状がある者に処方を検討することとされています。
- 本剤の成分に対し、重篤な過敏症の既往歴がないこと。
- 成人または12歳以上の小児であること。
- 併用禁忌の薬剤を投与していないこと。
- 腎機能または肝機能障害のある患者については、コルヒチンを投与していないこと。
- 妊婦又は妊娠している可能性のある女性ではないこと。
また、ゾコーバは、重症化リスク因子のある軽症例に対して、重症化抑制効果を裏付けるデータは得られていません。
重症化リスク因子のある患者に対しては、重症化予防に効果が確認されているラゲブリオ、パキロビッドなどによる治療を検討すべきとされていますので、次の重症化リスク因子(※)を有する者であって、医師が必要と判断した者については、他剤の処方をご検討ください。
※重症化リスク因子
- 65 歳以上の高齢者
- 悪性腫瘍
- 慢性呼吸器疾患(COPD など)
- 慢性腎臓病
- 糖尿病
- 高血圧
- 脂質異常症
- 心血管疾患
- 脳血管疾患
- 肥満(BMI 30 以上)
- 喫煙
- 固形臓器移植後の免疫不全
- 妊娠後半期
- 免疫抑制・調整薬の使用
- HIV 感染症(特に<CD4200/μL) など
(「診療の手引き 第8.1 版」が想定されます。処方にあたっては最新情報をご確認ください。)
(2)その他
- 3月31日以降の院内又は薬局内在庫として保有する国購入品の取り扱いについて
令和5年3月2日付け厚生労働省新型コロナウイルス感染症対策推進本部及び医薬・生活衛生局総務課事務連絡「新型コロナウイルス感染症における経口治療薬(ゾコーバ錠125mg)の薬価収載に伴う医療機関及び薬局への配分等について(その3)」に基づき患者に投与可能です。
チェックリスト等取り扱いが変更している点もありますので、令和5年5月22日付け厚生労働省新型コロナウイルス感染症対策本部、医薬・生活衛生局総務課の事務連絡「新型コロナウイルス感染症における経口抗ウイルス薬(ゾコーバ錠125mg)の取扱いについて(所有権の移転および再譲渡)」も確認してください。
薬務課HP(https://www.pref.yamaguchi.lg.jp/soshiki/48/20482.html)
- 同意書ひな形について
塩野義製薬株式会社の医療関係者向け情報ページ(https://www.shionogi.co.jp/med/products/drug_sa/xocova.html<外部リンク>)に掲載されています。
- 高齢者施設における対応について
高齢であることは、治療薬投与に当たっての重症化リスク因子の一つに含まれているため、重症化を抑制する効果のある薬剤の使用をご検討ください。
※山口県内のゾコーバ登録済医療機関一覧は以下のPDFファイルをご覧ください
【ゾコーバ】登録医療機関一覧 (PDF:483KB)
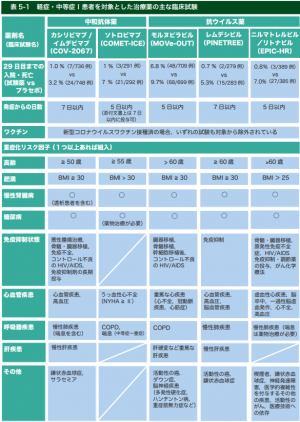
(出典:「新型コロナウイルス感染症(COVID19)診療の手引き・第9.0版」(令和5年2月17日)59頁 表5-1))